Chirurgie muco-gingivale des alternatives
Dossier du mois de Juillet 2024 - AO News #67

Introduction
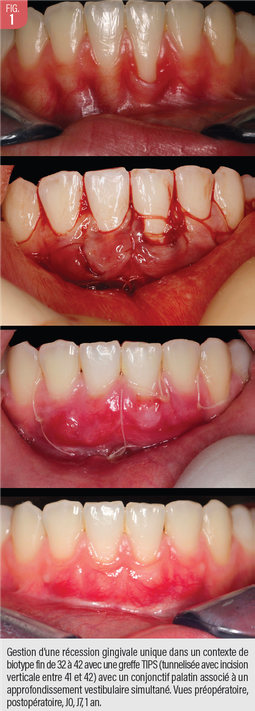
Le recouvrement des récessions gingivales se heurte fréquemment au risque supposé du prélèvement palatin (Fig. 1). Cette crainte peut être partagée par le praticien et le patient. De plus, la prévisibilité de la gestion des défauts gingivaux implique la compréhension étiologique de ces atrophies tissulaires.
Cette terminologie « atrophie » fait référence aux processus de souffrances cellulaires et de lésions de la matrice extra-cellulaire. Ces lésions sont caractérisées par une diminution qualitative ou quantitative de la population cellulaire et de leur fonction, résultant d'une agression cellulaire sublétale, telle que l'hypoxie, la compression mécanique, la vascularisation locale réduite, les remaniements trop rapides, les carences, l’épigénétique et autres facteurs non décodés.
Les causalités peuvent-être très diverses et il est essentiel de les identifier pour mieux les corriger en amont.
Analyse étiologique
- Facteurs anatomique/génétique biotype, hyper divergents, parafonctions, femmes …
- Facteur comportementaux (brossage traumatique…)
- Facteur inflammatoire bactérien : la plaque dentaire provoque une inflammation délétère qui associée aux collagénases bactériennes amoindrie l’attache.
- Orthodontie iatrogène : déplacement d’expansion trop rapide, trop prononcé…
- Hygiène de vie délétère (stress, dérèglements hormonaux, carences (4), IMC inférieur à
- 18,5, tabac…)
Nous devons imaginer qu’il existe forcément d’autres facteurs non connus ou non corrélés à ce jour. L’approche globale est donc indispensable, et tout miser sur la technique chirurgicale ou le choix du matériau ne peut suffire. Leur prise en compte pour expliquer la situation dans son
ensemble au patient avant tout acte chirurgical est essentielle pour corriger en amont de la greffe tout ce qui peut l’être.
Greffe autogènes
Différentes procédures sont actuellement largement décrites dans la littérature. La greffe conjonctive palatine enfouie est aujourd’hui le gold standard, qu’elle soit enfouie par tunnelisation ou placée sous un lambeau d’avancé coronaire (approche bilaminaire, Tavelli). De nombreuses variables ont été développées au cours des dernières années, venant confirmer des résultats supérieurs en termes de recouvrement comparativement aux techniques classiques de greffe gingivale libres. Le secteur mandibulaire antérieur est le sextant le plus exigeant pour lequel le choix d’un greffon autogène est de mise dans la majeure partie des indications.
Matrices de Derme Acellulaire (MDA)
Les substituts osseux ont connu un succès que les substituts gingivaux n’auront probablement jamais. Cependant, tout comme pour les régénérations osseuses guidées, les biomatériaux ont désormais une place légitime également pour la gestion des tissus mous. Comme le rapporte Ramos-Duron (5), les premières utilisations historiques des matrices de derme remontent à 1992 avec Alloderm© pour la gestion de grands brûlés. L’apport initial était de pouvoir se passer des impératifs histocompatibilité, et d’avoir en permanence du tissu donneur conservable, prêt et stérile. (6). En 1996, Shulman (7) publie la première évaluation clinique de MDA en épaississement de gencive attachée. Il utilise alors une MDA de type allogreffe destinée aux brûlés. Il décrit des avantages majeurs tels qu’une meilleure correspondance des couleurs et des contours, la diminution du nombre de chirurgies et l’absence de contrainte de dimensions liée habituellement à la taille du site donneur.
De nombreuses études comme celle de Lin (8) ont montré le potentiel d’activation de cicatrisation et migrations cellulaires au sein des matrices, tant au niveau des fibroblastes que des cellules desmodontales. En outre, il a montré la nécessité d’une excellente réhydratation pour permettre une optimale migration cellulaire au sein des matrices de derme. Un des mécanismes est d’absorber et de relarguer sur plus de 2 semaines des facteurs de croissance cellulaire suite à la chirurgie (9).
Les MDA sont représentées comme des échafaudages tissulaires bio actifs se substituant de façon prévisible aux greffes gingivales autogènes (10). Mais la réalité clinique est plus subtile, et impose de mettre en exergue les véritables avantages, particularités, et risques majorés pour une utilisation consciente et raisonnée (Fig. 2)
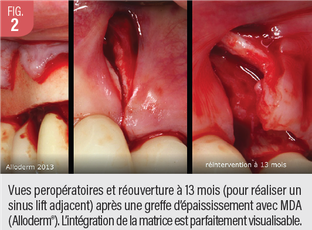
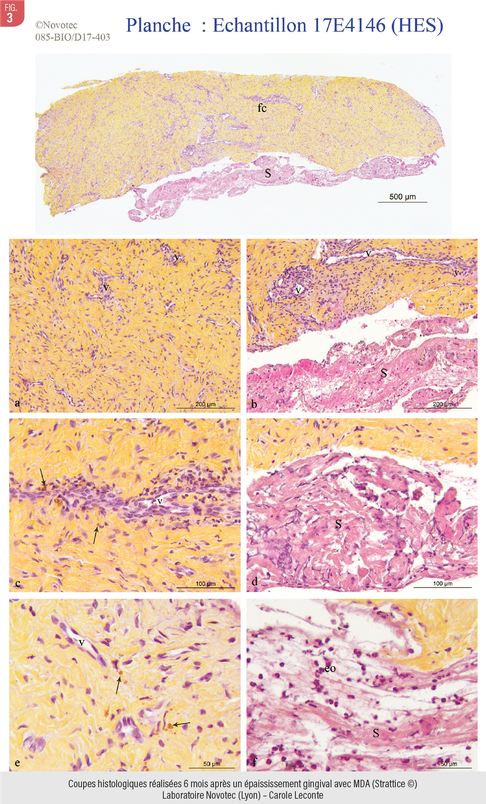
L’intégration tissulaire non inflammatoire des MDA, et leur colonisation par les cellules conjonctives et les néo-vaisseaux, fait que les analyses histologiques ne peuvent les distinguer d’un tissu fibrocellulaire dense natif (Fig. 3).
Choix de la technique chirurgicale
La phase initiale de préparation des racines exposées est essentielle et commune à toutes les techniques chirurgicales de greffe gingivales. Une élimination soigneuse d’éventuelles résines, puis mises en condition tissulaires doivent être réalisées juste avant la chirurgie. Passage des ultra-sons, puis aéropolissage, puis enfin préparation de la surface dentinaire avec un laser Erbium-YAG à faible puissance (50 mJ, 30 Hz) ou de l’EDTA à 24 % pour éliminer la smear layer. Ceci permet d’optimiser la ré-attache des fibroblastes (11). (Fig. 4)
MDA et lambeau
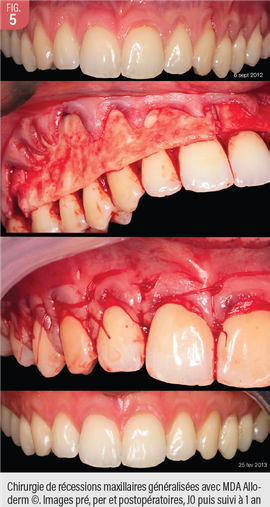
La technique du lambeau déplacé coronairement de Norberg (1926), associée à la mise en place d’une MDA est la technique la plus accessible et prévisible. L‘accès chirurgical gingival est plus naturel, le contrôle visuel est meilleur, notamment en cas de déhiscences sous un biotype très fin, et le décollement plus facile permet un gain de laxité plus généreux. La couverture sans tension du greffon est donc plus facilement obtenue. Cependant, les sections des papilles contribuent à une perte de prévisibilité esthétique à ce niveau, et la laxité du lambeau impose des techniques de sutures spécifiques assurant un repositionnement coronaire stable des greffons et du lambeau (Fig. 5).

MDA et Tunnel
Les techniques tunnelisées permettent de s’affranchir de la section des papilles. La technique décrite par Allen (1984) ne peut être utilisée comme telle avec les matrices. En effet, la rigidité et la largeur des bandelettes de MDA ne sont pas compatibles avec une insertion par le sulcus. L’incision distale proposée en 2001 par Santarelli corrige en partie cette limite mais ne permet ni un accès confortable pour le décollement, ni une insertion aisée. Cette technique indiquée avec les prélèvements autogènes est incompatible avec les matrices. La mata analyse de Tavelli (12) confirme les travaux de Zucchelli en constatant que même si la technique tunnelisée traditionnelle est fiable, les statistiques sont en faveur des techniques avec lambeau déplacé coronairement, associées à un greffon (autogène ou MDA). Dans les statistiques retenues, le taux de recouvrement radiculaire est supérieur qu’en technique tunnelisée. Cependant, l’essai clinique randomisé de Zuhr a montré l’inverse. La maitrise technique a conduit à un taux de couverture de racine exceptionnel de 98,4% en tunnelisé, contre 71,8% en lambeau déplacé associé à une greffe (13, 14).
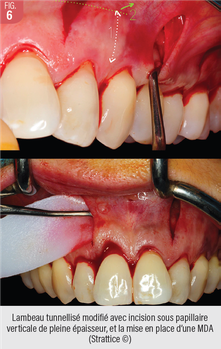
Technique TISP (Tunnelisée avec Incision Sous Papillaire)
Cette approche que j’ai développée depuis 2013 fait appel à 4 incisions de décharges sous papillaires de pleine épaisseur au niveau alvéolaire, étendue en demi épaisseur en regard du replis vestibulaire (Fig. 6 à 8). Cette incision verticale interdentaire sous papillaire doit rester à 2mm du sulcus, et permet un décollement strict de pleine épaisseur. Ceci évite de fragiliser les biotypes fins, ce qui pourrait être à l’origine de déhiscence des MDA ou de nécroses de surface, surtout en cas d’utilisation d’une matrice trop dense, épaisse ou rigide. L’insertion du greffon de MDA est alors possible de l’avant vers l’arrière sans traumatiser le lambeau. Dans cette approche avec incision verticale, le rôle des décolleurs est essentiel. Pour limiter le nombre d’incisions verticales sous papillaires et gérer parfaitement des lambeaux de pleine épaisseur sur des grandes portions d’arcades, des instruments à double design et aux parties travaillantes optimisées ont été créés en collaboration avec la société DEVE (Fig. 7).
Les parties latérales sont légèrement émoussées pour limiter le risque de déchirure des papilles. Les proportions rallongées permettent un accès distal plus aisé.
Cette technique nécessite peu de sutures :
- la réalisation des sutures suspendues est fortement conseillée pour le maintien vertical des matrices et leur recouvrement par la muqueuse alvéolaire,
- ces sutures peuvent être réalisées avec du PGA rapide 5/0, en pont autour des dents,
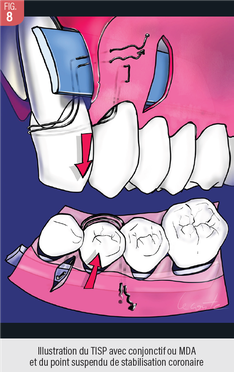
- cette technique est simple, rapide, ne nécessite pas de collage interproximaux ou vestibulaire, et ne laisse pas de cicatrices (Fig. 8).


Discussion
Taux de recouvrement : les études de Pietruska (15) et Cieslik et Wegemund (16) mesurant les taux de couverture complète des récessions avec prélèvements autogènes versus MDA sont particulièrement dissonantes.
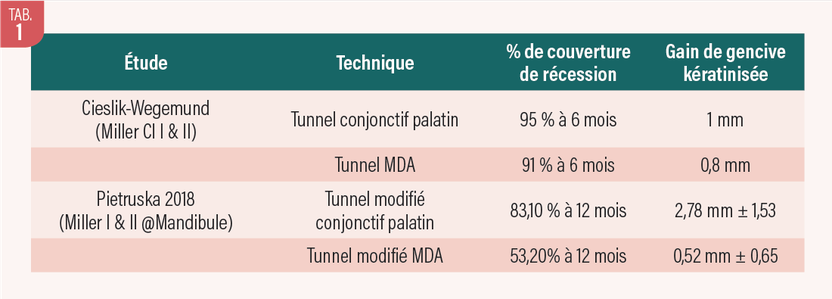
Si des différences selon les protocoles et matériaux sont soulignés par la méta-analyse de Dadlani (16), les résultats sont toujours plus favorables avec l’autogène. Dans notre expérience, ceci se confirme principalement au niveau des greffes mandibulaires. De plus, le risque de récidive verticale (nouvelle récession) ou horizontale (en épaisseur) est supérieur avec les biotypes fins (11). Il paraît donc opportun de ne pas attendre des situations trop avancées pour corriger les atrophies gingivales.
Intérêts et limites
Dans le secteur mandibulaire antérieur, la faible vascularisation terminale, les tensions, ainsi que le phénotype particulièrement fin (gencives et tables vestibulaires), sont autant de facteurs de risques qui diminuent la prévisibilité et la pérennité de l’utilisation de MDA. Le palais représente ainsi le choix de première intention tant que le volume à corriger est compatible. Les prélèvements autogènes montrent une variété de densité fibreuse. Ainsi la présence d’un tissus conjonctif riche et dense en collagène sera extrêmement favorable, donnera un greffon facile à manipuler et une très bonne stabilité dans le temps. Les MDA proposent une quantité non limitée et une qualité assez constante conduisant à une harmonie de volume et de couleur généralement plus favorable que les greffes autogènes sur les défauts de grande étendue.
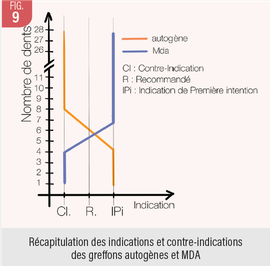
Les matrices, après réhydratation longue, sont faciles à glisser sous le périoste, et leur densité permet un soutien spontané partiel des tissus. La MDA nous permet d’aborder plus sereinement des secteurs de grandes étendues. Le greffon autogène sera à privilégier dans les récessions de faibles étendues (Fig. 9) ou en combinaison avec les matrices.
Différents types de MDA
Les différentes matrices disponibles, du fait de leur mode de production, ont des comportements très différents. Le type de donneur (humain, porcin, bovin), l’âge ou le stade fœtal, les procédures de traitement ou encore le mode de conservation (lyophilisé ou fixateur) vont considérablement influencer le comportement biologique. Ainsi les proportions de collagène de type I et III vont varier, l’épaisseur, la rigidité /densité sont à appréhender. Globalement, plus elles sont rigides et denses, plus la stabilité dimensionnelle est grande, mais plus les risques d’exposition ou de nécrose superficielle sont grands. Selon la nature du collagène et le traitement, la cicatrisation conduit plutôt vers une intégration ou plutôt vers une résorption. Limiter les mécanismes inflammatoires grâce à un traitement optimal, assurant la sécurité en éliminant toute trace cellulaire et préserver les qualités du collagène est ainsi essentiel. Les comportements des MDA sont donc très divergents d’un procédé à l’autre, même au sein de matériaux d’origine commune. Un compromis épaisseur, rigidité, revascularisation, résorption est donc essentiel en parodontologie, mais également la lecture attentive des coupes histologiques des biomatériaux et des cicatrisations.
Notre expérience nous a montré que les résultats les plus prévisibles et pérennes étaient en Alloderm® (malheureusement interdite en france), puis en Novomatrix®. La Surgimend® 2mm a un bon comportement au maxillaire mais le remaniement est plus aléatoire, notamment souvent décevant à la mandibule. La Strattice® a également apporté une certaine satisfaction mais cette dernière ne tient pas bien la comparaison face aux deux premières matrices citées. Les autres MDA que nous avons pu utiliser ne nous ont pas apporté une satisfaction suffisante.
Ré-attache cellulaire et stabilité du volume
À court terme, la cicatrisation présente une phase initiale avec une ré-attache qui se met en place les 3 premiers mois par migrations cellulaires et synthèses de protéoglycanes. La maturation se termine vers les 6 mois après la greffe, marquant une stabilisation du volume et niveau obtenu (18). Le vieillissement des zones greffées est meilleur que les sites non greffés, mais le temps agit quand même sur ces tissus comme sur le reste de l’organisme.
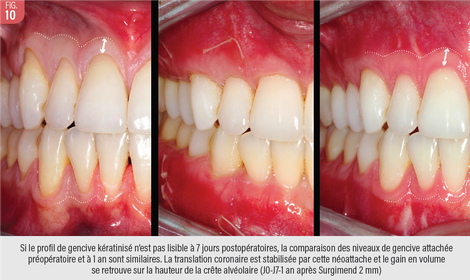
Le gain de gencive kératinisé après MDA
L’analyse des nombreux patients opérés avec matrices de derme met en évidence l’importance de la qualité du tissus receveur pour définir la future qualité de la gencive attachée. La présence de gencive kératinisée résiduelle, même fine, est un facteur très favorable. En effet, les cellules de la gencive décollée vont coloniser la matrice et définir ainsi le futur niveau de gencive kératinisée. Ceci met en exergue l’importance de ne pas retarder trop la prise en charge des patients afin de ne pas perdre toute la gencive adhérente résiduelle (Fig. 10).
Résorption et MDA
Un suivi à long terme (19) a mis en évidence que le taux moyen de couverture des récessions à 4 ans était significativement inférieur à celui obtenu à 12 mois. La sélection de traitements de récessions multiples et adjacentes localisées dans le secteur mandibulaire antérieur constitue manifestement un biais de sélection aggravant les résultats en défaveur des MDA sur ce secteur. Barootchi (20) a comparé à 9 ans l’évolution des niveaux et volumes gingivaux des sites greffés avec MDA et des sites adjacents non traités. Le déplacement apical était systématiquement plus marqué dans les sites non greffés.
Exposition
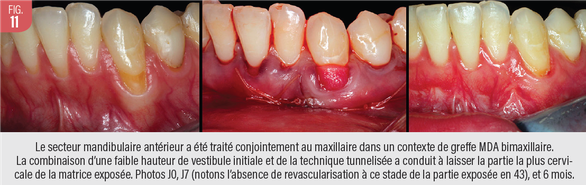
La MDA nécessitant une croissance tissulaire en son sein, l’exposition montre un risque de résorption plus marqué (21), mais la croissance conjonctive au sein de la matrice n’est pas bloquée (Fig. 11). L’exposition reste contre-indiquée. Un soin particulier à donner une laxité généreuse est essentiel, conjointement à une stabilisation efficace par les sutures suspendues.
Risques d’exposition non volontaire
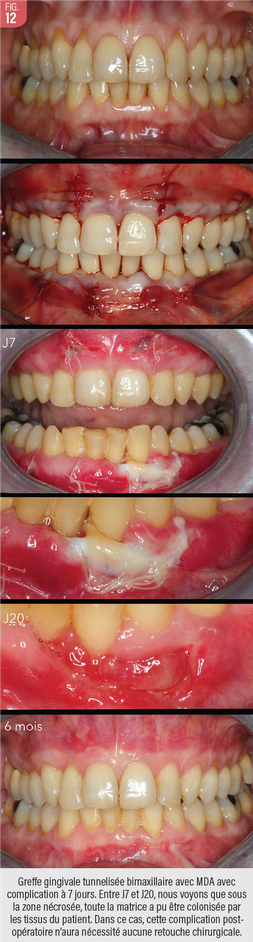
La combinaison de biotypes fin, atrophiques et de matrices de grande dimension, denses, épaisses et hautes, augmentent le risque d’exposition secondaire par nécrose du plan superficiel (Fig. 12). Cette complication rare dans notre expérience (4 cas en 12 ans) s’est toujours soldée par une issue favorable ou acceptable sans intervention. Une amélioration dans un deuxième temps avec un greffon palatin a parfois été réalisé pour optimiser le résultat. Il est nécessaire de préserver la capacité de cicatrisation du patient et de croissance cellulaire en limitant les premiers jours l’application de chlorhexidine qui est cytotoxique sur les fibroblastes, et de laisser sans contraintes la matrice le temps qu’elle soit colonisée par les néo-vaisseaux.
Conclusion
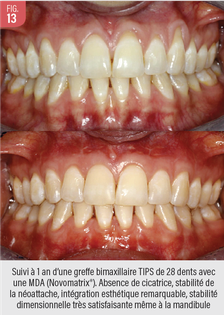
Actuellement, le recouvrement radiculaire est de plus en plus prévisible. Cette prise en charge doit être suffisamment précoce. Pour tous les défauts d’une taille compatible avec un prélèvement autogène, le prélèvement palatin doit être la règle. Les MDA constituent une alternative qui prend tout son sens pour la gestion des défauts de grandes étendues. L’analyse du biotype résiduel, la maitrise de la technique, le choix du type de matrice, et la prise en compte du terrain sont alors essentiels. Une situation de recessions généralisées avec pertes marquées sur le bloc mandibulaire antérieur peut nous conduire à combiner l’utilisation des matrices complétées par un prélèvement palatin. Le pronostic et la pérennité de ces techniques sont multifactoriels. Ils dépendent notamment du type de matrice utilisée, de la technique réalisée, et de la qualité de cicatrisations des patients. La technique tunnelisée TISP constitue une amélioration de la prise en charge chirurgicale non négligeable (Fig. 13).
Bibliographie :
1. Slutzkey S, Levin L. Gingival recession in young adults: occurrence, severity, and relationship to past orthodontic treatment and oral piercing. Am J Orthod Dentofacial Orthop. 2008 Nov;134(5):652-6..
2. Ji JJ, Li XD, Fan Q, Liu XJ, Yao S, Zhou Z, Yang S, Shen Y. Prevalence of gingival recession after orthodontic treatment of infraversion and open bite. J Orofac Orthop. 2019 Jan;80(1):1-8.
3. Roussarie F, Douady G, Effets indésirables des fils de contention collés : le « syndrome du fil » 1re partie, Rev Orthop Dentofaciale 2015;49(4):411-426.
4. Moores J. Vitamin C: a wound healing perspective. Br J Community Nurs. 2013 Dec;Suppl:S6, S8-11
5. Ramos Duron LE, Martínez Pardo ME, Olivera Zavaleta V, Silva Diaz T, Reyes Frías ML, Luna Zaragoza D. Application of acellular dermis and autograft on burns and scars. Ann Transplant. 1999;4(3-4):74-7
6. Wainwright D, Madden M, Luterman A, Hunt J, Monafo W, Heimbach D, Kagan R, Sittig K, Dimick A, Herndon D. Clinical evaluation of an acellular allograft dermal matrix in fullthickness burns. J Burn Care Rehabil. 1996 Mar-Apr;17(2):124-36
7. Shulman J. Clinical evaluation of an acellular dermal allograft for increasing the zone of attached gingiva. Pract Periodontics Aesthet Dent. 1996 Mar;8(2):201-8.
8. Lin Z, Nica C, Sculean A, Asparuhova MB. Enhanced Wound Healing Potential of Primary Human Oral Fibroblasts and Periodontal Ligament Cells Cultured on Four Different Porcine-Derived Collagen Matrices. Materials (Basel). 2020 Aug 29;13(17):3819.
9. Nica C, Lin Z, Sculean A, Asparuhova MB. Adsorption and Release of Growth Factors from Four Different Porcine-Derived Collagen Matrices. Materials (Basel). 2020 Jun 9;13(11):2635.
10. Tavelli L, McGuire MK, Zucchelli G, Rasperini G, Feinberg SE, Wang HL, Giannobile WV. Extracellular matrix-based scaffolding technologies for periodontal and peri-implant soft tissue regeneration. J Periodontol. 2020 Jan;91(1):17-25. doi: 10.1002/JPER.19-0351. Epub 2019 Sep 19.
11. Bolortuya G, Ebihara A, Ichinose S, Watanabe S, Anjo T, Kokuzawa C, Saegusa H, Kawashima N, Suda H. Initial fibroblast attachment to Erbium:YAG laser-irradiated dentine. Int Endod J. 2011 Dec;44(12):1134-44.
12. Tavelli L, Barootchi S, Nguyen TVN, Tattan M, Ravidà A, Wang HL. Efficacy of tunnel technique in the treatment of localized and multiple gingival recessions: A systematic review and meta-analysis. J Periodontol. 2018 Sep;89(9):1075-1090.
13. Zuhr O, Rebele SF, Schneider D, Jung RE, Hürzeler MB. Tunnel technique with connective tissue graft versus coronally advanced flap with enamel matrix derivative for root coverage: a RCT using 3D digital measuring methods. Part I. Clinical and patient-centred outcomes. J Clin Periodontol. 2014 Jun;41(6):582-92.
14. Rebele SF, Zuhr O, Schneider D, Jung RE, Hürzeler MB. Tunnel technique with connective tissue graft versus coronally advanced flap with enamel matrix derivative for root coverage: a RCT using 3D digital measuring methods. Part II. Volumetric studies on healing dynamics and gingival dimensions. J Clin Periodontol. 2014 Jun;41(6):593-603.
15. Pietruska M, Skurska A, Podlewski Ł, Milewski R, Pietruski J. Clinical evaluation of Miller class I and II recessions treatment with the use of modified coronally advanced tunnel technique with either collagen matrix or subepithelial connective tissue graft: A randomized clinical study. J Clin Periodontol. 2019 Jan;46(1):86-95.
16. Dadlani S. Porcine Acellular Dermal Matrix: An Alternative to Connective Tissue Graft-A Narrative Review. Int J Dent. 2021 Sep 6;2021:1652032
17. Imber JC, Kasaj A. Treatment of Gingival Recession: When and How? Int Dent J. 2021 Jun;71(3):178-187. doi: 10.1111/idj.12617. Epub 2021 Jan 29.
18. Rebele SF, Zuhr O, Schneider D, Jung RE, Hürzeler MB. Tunnel technique with connective tissue graft versus coronally advanced flap with enamel matrix derivative for root coverage: a RCT using 3D digital measuring methods. Part II. Volumetric studies on healing dynamics and gingival dimensions. J Clin Periodontol. 2014 Jun;41(6):593-603.
19. Cosgarea R, Miron R, Bora R, Rosu A, Buduru S, Sculean A. Long-term results after treatment of multiple adjacent gingival recessions with the modified coronally advanced tunnel and a porcine acellular dermal matrix. Quintessence Int. 2021;52(1):32-44
20. Barootchi S, Tavelli L, Gianfilippo RD, Eber R, Stefanini M, Zucchelli G, Wang HL. Acellular dermal matrix for root coverage procedures: 9-year assessment of treated isolated gingival recessions and their adjacent untreated sites. J Periodontol. 2021 Feb;92(2):254-262.
21. Boháč M, Danišovič Ľ, Koller J, Dragúňová J, Varga I. What happens to an acellular dermal matrix after implantation in the human body? A histological and electron microscopic study. Eur J Histochem. 2018 Jan 22;62(1):2873.

